|
V.
Debreceni Kardiol¾giai Napok
2000. mßrcius
2 - 4. Debrecen — DOTE
|
|
a teljes elõadás hangfelvétele: |
Dr. Forster Tamás (Szeged) |
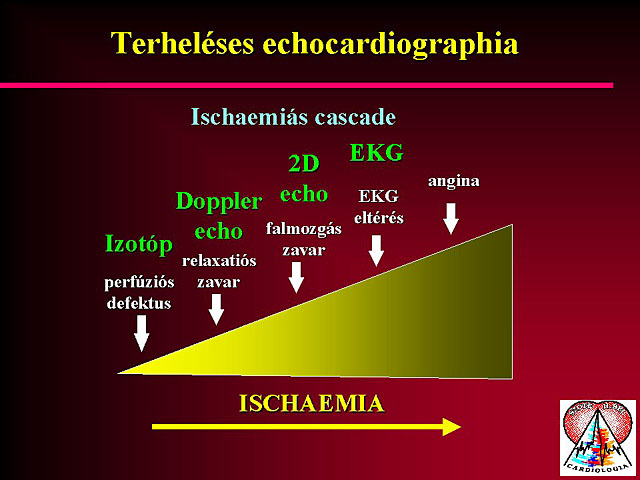
Az ischaemiás szívbetegség továbbra is vezetõ szerepet tölt be a halálokok között. Számos ember haláláért, illetve rokkantságáért felelõs, ezért a mûtétet igénylõ betegek idõbeni felderítése a kardiológiai diagnosztika egyik fontos területe. Ischaemiát számos stimulussal lehet provokálni, és a kiváltott ischaemiát számos módszerrel lehet detektálni. Ezt az ischaemiás cascade segítségével lehet jól jellemezni. Míg a coronarographia csak morphologiai, statikus információt ad, addig a terheléses vizsgálatok dinamikusan értékelik a koszorúér betegség haemodynamikai következményeit.
1. Terheléses echocardiographia
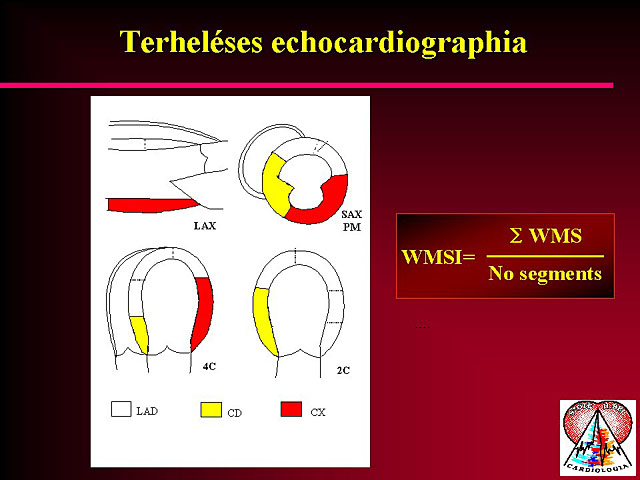
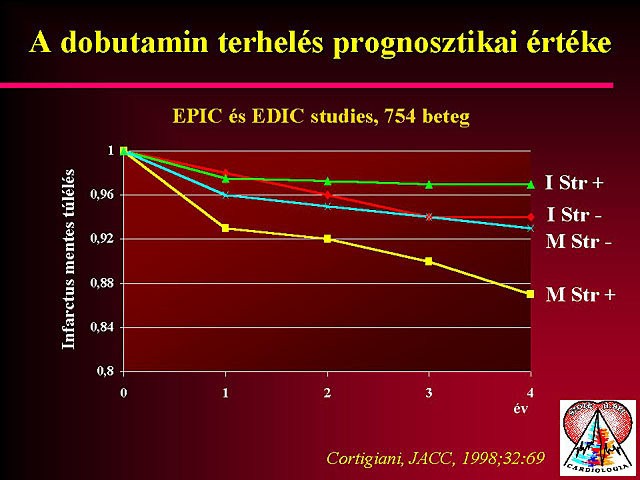
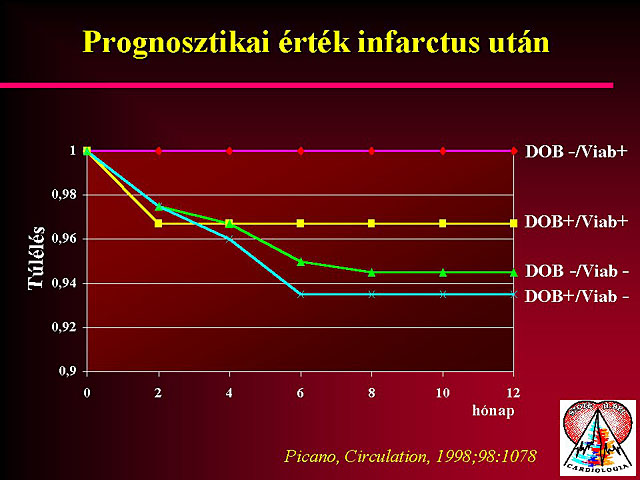
A terheléses echocardiographia az ischaemiás szívbetegség kimutatásának egyre szélesebb körben alkalmazott módszere. A kiváltott ischaemiát a falmozgászavarok detektálása útján tudja regisztrálni. A falmozgás score index (a bal kamra segmentális beosztása) segítségével nemcsak az ischaemia súlyossága ítélhetõ meg az adott területen, hanem a betegség kiterjedése is. A módszer az ischaemia kimutatása mellett alkalmas a myocardium életképességének felderítésére is. A falmozgászavarok megítélése az echocardiographiás diagnosztika egyik legnehezebb, legproblematikusabb feladata. Az echocardiographiára általában is igaz, hogy nagy gyakorlatot igényel, de ez a megállapítás még fokozottan igaz a falmozgászavarok megítélésére. Ettõl a vizsgálat értékelése szubjektív és nehezen reprodukálható lesz. Új módszereket vezettek be, melyek a terheléses echocardiographiás vizsgálatok értékelését egyszerûbbé és objektívabbá teszi. Ilyen módszer a szöveti Doppler echocardiographia és a color kinesis.
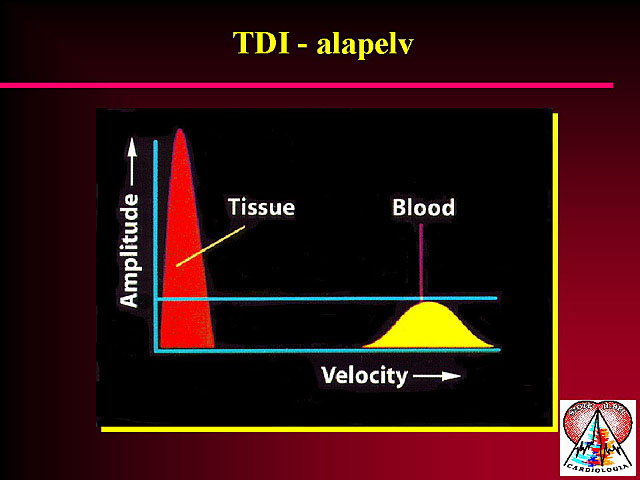
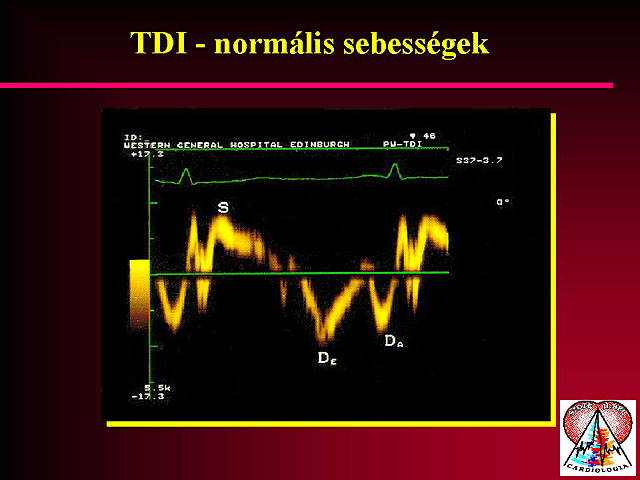
2. Szöveti Doppler echocardiographia
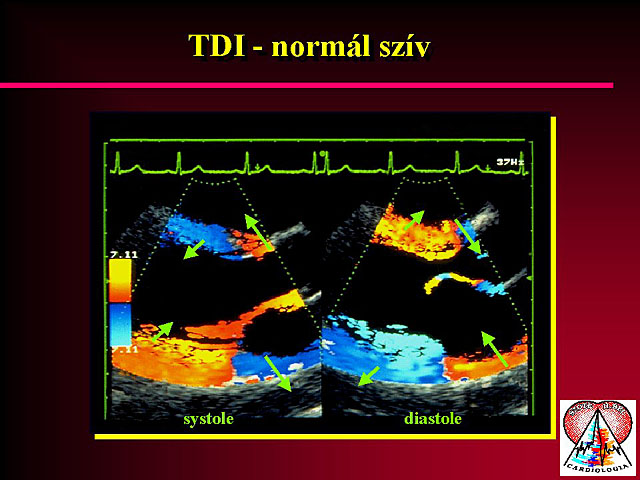
A szöveti Doppler echocardiographia alapelve megfordítja a színes Dopplernél alkalmazott szûrõzési elvet. Amíg a színes Dopplernél az ún. ähigh pass filterö a nagysebességû komponenst, a vér által kiváltott jelet ereszti át, míg a szöveti Dopplernél a kis sebességû, de nagy amplitúdójú jeleket regisztráljuk, mely a falról verõdik vissza. A kapott információt kétféle formában is megjeleníthetjük. Egyrészt a fal mozgását színezve ábrázolhatjuk, ahol a színkódolás elve azonos a színes Doppleréval (a transducer felé mozduló falrészlet piros, az elfelé mozduló kék színben kódolódik). Másrészt az adott terület pulzatilis Doppler spektrumát regisztrálhatjuk. Akár a színek, akár a pulzatilis Doppler spektrum alapján szegmentumonként értékelhetjük a szív egyes régióinak falmozgását. Nyugalomban és terhelés során is elemezhetjük a falmozgászavarokat, illetve azok jellemzõit. A szöveti Doppler echocardiographia alkalmas a myocardium életképességének a megítélésére, illetve a ritmuszavarok elemzésére is. A módszert részleteiben külön kerül bemutatásra.
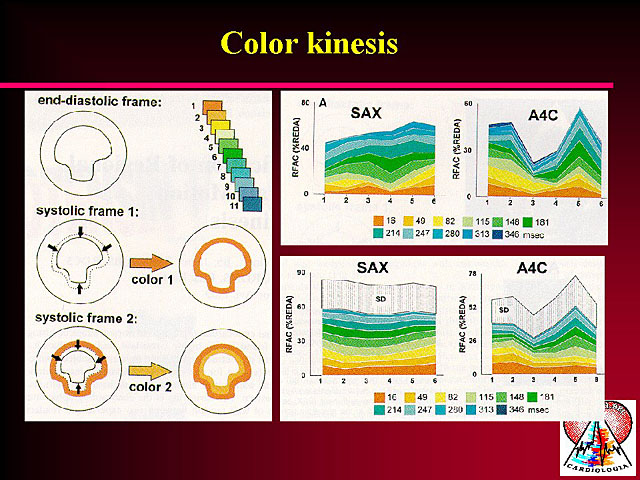
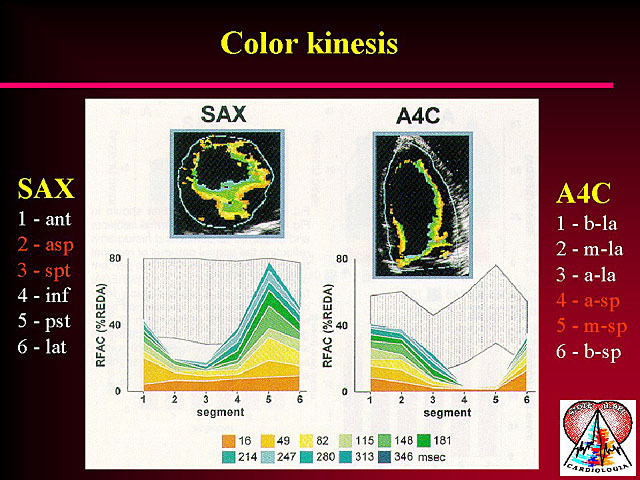
3. Color kinesis
Egy másik technika, mellyel a falmozgászavarok pontosabban megítélhetõvé vállnak, a color kinesis. Az akusztikus quantificatió és az automatikus kontúrdetekció alapján a vér-szövet határ meghatározható, majd a fal bizonyos idõnkénti elmozdulása különbözõ színekkel beszínezhetõ. Az összesített kép alapján képet kaphatunk a falmozgás amplitúdójáról és sebességérõl. Ha falmozgászavar, pl. hypokinesis áll fenn, a fal elmozdulása kisebb mértékû lesz, melyet könnyen észrevehetünk. Akinesis esetén egyáltalán nem látunk elmozdulást, ilyenkor színkód sem jelenik meg. Egy speciális kapcsoló segítségével a hypo- és akinesis mellett a dyskinesist is megjeleníthetjük. Tekintettel arra, hogy minden egyes ember falmozgása különbözik, így érdemes felállítani egy adatbázist, melybe egészséges egyének adatait táplálják be, majd ezt követõen meghatározhatják a normális tartomány határait. Ez alapján a határértékeket meghaladó elmozdulást lehet kórosnak tartani. A módszer alapvetõ problémája, hogy csak azokban a készülékekben használható, ahol az akusztikus quantificatiót beépítették, ez pedig csak néhány típusban található meg. A másik probléma az, hogy csak a falszegmentumok elmozdulását lehet ilyen formában kiértékelni, de a fal belsõ ätulajdonságairólö további információt nem kapunk. A szöveti Doppler echocardiographia módszere minden készülékbe beépíthetõ és információ tartalma is jóval nagyobb, ezért gyorsabban is terjed a módszer.
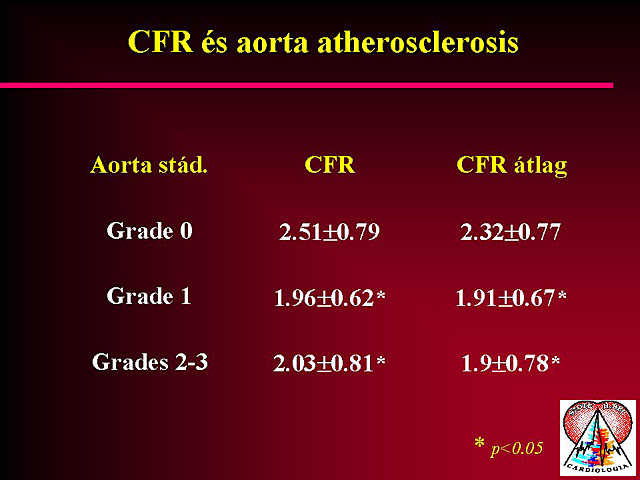
4. Coronaria áramlási reserve vizsgálata
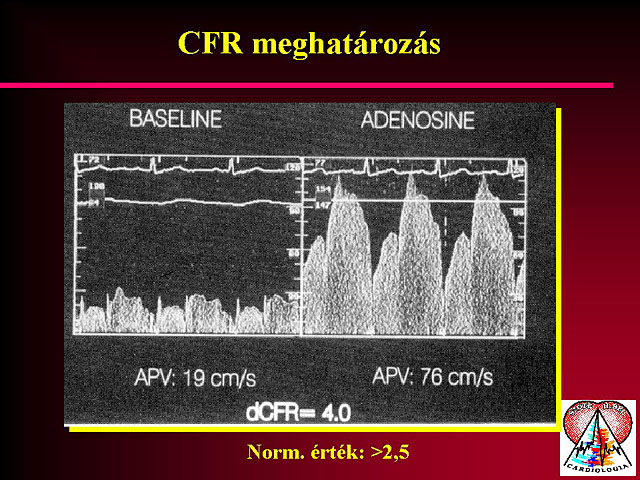
A coronaria áramlási reserve a coronariáknak valamilyen stimulus hatására (pl. vasodilatáció) bekövetkezõ alkalmazkodóképességét jellemzi. Egy jól reagáló koszorúér esetén az áramlás akár a 3-4-szeresére is megnövekedhet.
Az epicardialis coronariák szûkülete miatt az áramlási nagyobb rezisztencia ellenében történik, ezért az áramlás vasodilatátor stimulus hatására csak kisebb mértékben emelkedik meg. Vasodilatatorként adhatunk dipyridamolt vagy adenosint, mert mindkettõ hathatósan tágítja a koszorúér rendszert. Transoesophagealis echocardiographiás vizsgálat során a ramus descendens anterior proximális szakaszában nyugalomban és maximális vasodilatatió idején áramlási sebességet mérünk. A coronaria áramlási reserve (CFR) a maximális vasodilatáció idején mért áramlási sebesség és a nyugalmi áramlási sebesség hányadosa. A ramus descendens anterior szignifikáns szûkülete esetén a CFR értéke jelentõsen alacsonyabb lesz. Bizonytalan súlyosságú szûkület esetén a módszer alkalmas a szûkület szignifikanciájának megítélésére. Sikeres PTCA-t követõen a CFR értéke emelkedik, normalizálódik. Restenosis esetén újra csökken az áramlási reserve, így a CFR mérése alapján nagy biztonsággal kiválaszthatjuk ezen betegeket. A CFR értékét nemcsak az epicardialis coronariák szûkülete, hanem a microvasculatura károsodása is befolyásolja. X-syndroma esetén a CFR értéke szignifikánsan alacsonyabb még a ramus descendens anterior szûkületéhez képest is. Csökkenti a CFR értékét a bal kamra hypertrophia is, amikor a microvascularis rezisztencia szintén megemelkedik. Ilyent tapasztalhatunk aorta stenosisban, hypertrophiás cardiomyopathiában is. Önmagában a CFR nem ad elég információt a koszorúerek állapotáról, de hasznosan kiegészíti egyéb noninvazív vizsgálati módszereinket.
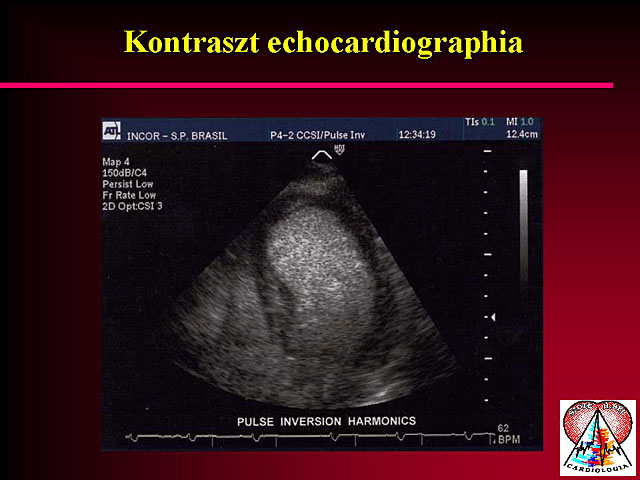
5. Kontraszt echocardiographia
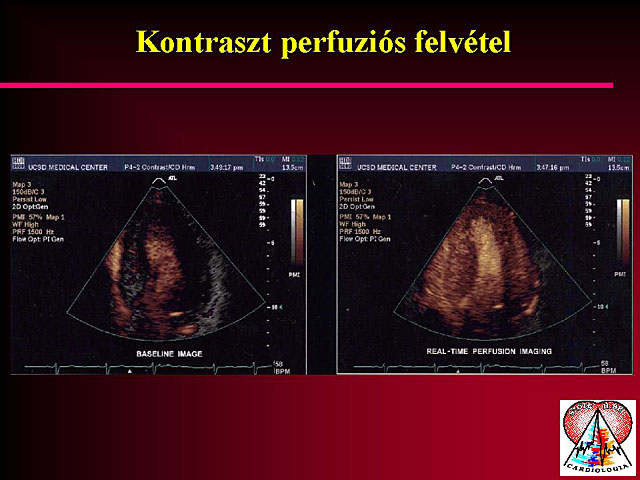
A kontraszt echocardiographia alapelve az, hogy bizonyos anyagokból mikrobuborékok szabadulnak fel, melyeknek az echogenitása fokozott, és ezt a szívüregekben egy äfehéres füstö formájában láthatjuk. Manapság számos olyan kontrasztanyagot állítanak elõ, melyek már átjutnak a tüdûn, ezért perifériás vénába beadva is feltelítik a balszívfelet (az új kontrasztanyagok buboréknagysága megegyezik a vvt-k nagyságával, ezért képesek átjutni a tüdõn). Ráadásul még a coronariakeringésbe is bekerülnek. A kontrasztanyaggal feltöltött myocardium echoreflektivitása megnövekszik a perfundált myocardium területekben. Myocardialis infarctus esetén az elzáródás mögötti területre nem jut kontrasztanyag, a két terület közötti különbség jól látható lesz. Thrombolysis után a recanalisatió igazolható kontraszt echocardiographiával. Nagyon jól demonstrálható a äno-reflowö-phenomenon is ezzel a módszerrel. Ilyenkor a sikeres thrombolysis és az átjárható infarctus-arteria ellenére sem indul meg a perfúzió. Az echocardiographiás technika sokat fejlõdött az utóbbi években. A jobb képalkotás érdekében a kontraszt echocardiographiás vizsgálatokhoz az ún. második felharmonikust is regisztrálni képes készülékek a megfelelõek. Ez a technika az ultrahangrezgés felharmonikusát detektálja, ezzel kiszûrve és csökkentve az alapzajt. Az ultrahang mechanikus energiája szétrobbantja a mikrobuburékokat és a kontraszt jelenség néhány másodperc alatt megszûnik. Intermittáló ultrahang energiaközvetítés megnöveli a buborékok élettartalmát, és így hosszabb idõ marad arra, hogy a myocardium is kellõképpen feltelõdjön. Számos klinikai szituációban próbálták már ki a kontraszt echocardiographia technikáját, de még mindig nem történtek olyan vizsgálatok, melyek a módszer helyét a napi rutinban megmutatnák.
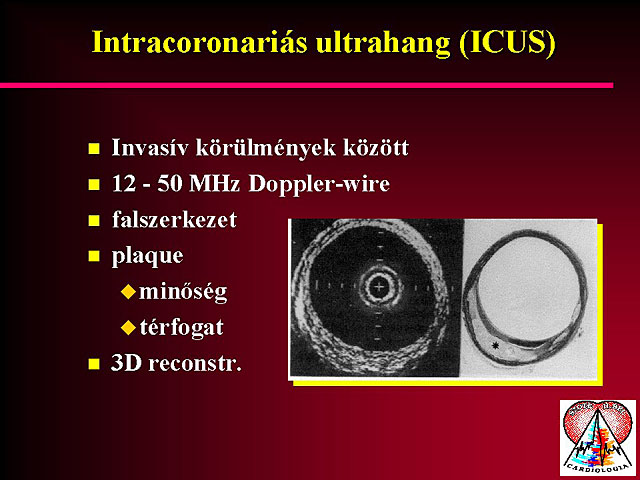
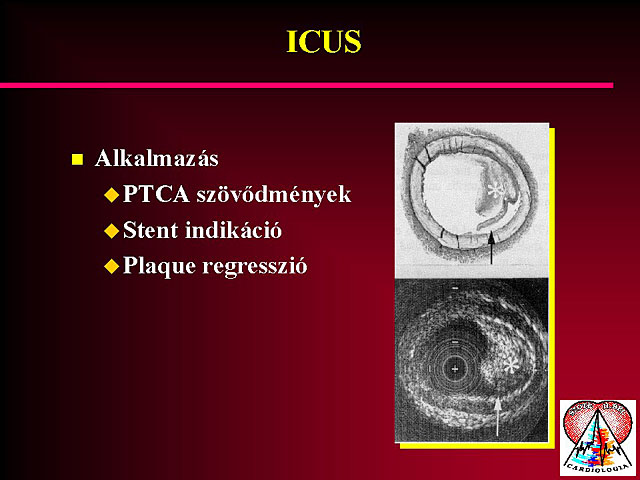
6. Intracoronariás ultrahang
Bár az intracoronariás vagy intravascularis ultrahangot csak invazív körülmények között lehet használni, mégis alapelvét tekintve az ultrahangos technikák sorába tartozik. Az itt használt miniatûr transducerek frekvenciája 12 és 50 MHz között mozog. Ilyen nagy frekvencia mellett a felbontóképesség sokkal jobb, a coronariák falszerkezete is ábrázolható. Látható a coronaria plaque, sõt annak összetételérõl is képet kaphatunk. Az intracoronariás ultrahang nem kifejezetten ischaemia kimutatására alkalmas, de coronariák morphologiáját sokkal pontosabban ábrázolja. Felhasználható pl. a PTCA szövõdményeinek felderítésére, segítségével pontosabban eldönthetõ, hogy kik azok a betegek, akiknek stent beültetésre van szüksége. Segít a szövõdményes esetek kiválasztásában, alkalmazásával optimalizálható a stentek használata. Alapvetõ probléma a módszerrel kapcsolatban az, hogy ezek az intracoronariás katéterek még mindig nagyon drágák, az áruk vetekedik a stentek árával, így alkalmazásuk csak megfelelõ finanszírozás mellett képzelhetõ el. Hazai viszonylatban az ex juvantibus stent beültetés még mindig olcsóbb, mint a racionális intracoronariás Doppler katéterek használata. Az intracoronariás Doppler és komputer technika együttes alkalmazásával a coronaria plaque mérete meghatározható, és az antilipaemiás kezelést követõen a plaque regressziója is jól követhetõ. Az atherosclerosis folyamata során a remodelling fázisban az ér lumene még nem szûkül lényegesen, de a falszerkezet már kóros eltéréseket mutat. Már ezt a stádiumot is jól lehet vizsgálni az intravascularis technika segítségével. Az intracoronariás ultrahang vizsgálat relatív drágásága miatt egyelõre még nem lehet a napi rutin vizsgálatok része hazánkban, bár várható, hogy az elkövetkezõ években itt lesz némi elõremozdulás.
Az echocardiographiás technikák számos válfaja alkalmazható az ischaemiás szívbetegek vizsgálatában, sok hasznos, klinikai értékõ információt kaphatunk tõlük, de manapság még nem helyettesíthetik a coronarographiát, sõt várhatóan ez közeljövõben nem is következik be. A két módszer kiegészíti egymást, mert a coronarographia csak morphológiai információt ad a koszorúerekrõl, míg az echocardiographiás technikák a coronariák funkcionális állapotáról adnak képet.Irodalom
1.) Hoffmann R., Lethen H., Marwick T., Arnese M., Fioretti P., Pingitore A., Picano E., Buck T., Erbel R., Flachskampf F.A., Hanrath P. Analysis of interinstitutional observer agreement in interpretation of dobutamin stress echocardiography. J Am Coll Cardiol, 1996; 27: 330-336.
2.) Bach DS, Armstrong WF, Donovan CL, Muller DW. Quantitative Doppler tissue imaging for assessment of regional myocardial velocities during transient ischemia and reperfusion. Am. Heart J., 1996; 132: 721-725.
3.) Gorcsan J, Gulati VK, Mandarino WA, Katz WE. Color-coded measures of myocardial velocity throughout the cardiac cycle by tissue Doppler imaging to quantify regional left ventricular function. Am. Hear. J., 1996; 131: 1203-1213.
4.) Lang RM, Vignon P, Weinert L, Bednarz J, Korcarz C, Sandelski J, Koch R, Prater D, Mor-Avi V. Echocardiographic quantification of regional left ventricular wall motion with color kinesis. Circulation, 1996; 93: 1877-1885.
5.) Schwartz SL, Cao QL, Vannan MA, Pandian NG. Automatic backscatter analysis of regional left ventricular systolic function using color kinesis. Am. J. Cardiol., 1996; 77: 1345-1350.
6.) Iliceto S., Marangelli V., Memurola C. et al.: Transesophageal Doppler echocardiography evaluation of coronary blood flow velocity in baseline conditions and during diypridamole-induced coronary vasodilation. Circulation, 1991; 83:
61-69.7.) Redberg R.F., Sobol Y., Chou T.M. at al.: Adenosine-induced coronary vasodilation during transoesophageal Doppler echocardiography. Rapid and safe measurement of coronary flow reserve ratio can predict significant left anterior descending coronary stenosis. Circulation, 1995; 92: 191-196.
8.) Kaul S.: Clinical application of myocardial contrast echocardiography. Am. J. Cardiol., 1992; 69: 46H-55H.
9.) Ragosta M., Camarano G., Kaul S. et al.: Microvascular integrity indicates myocaellular viability in patients with recent myocardial infarction. Circulation, 1994; 89: 2562-2569.
10.) Bassand J.-P.: Intravascular ultrasound guided PTCA: a way to escape stent mania. Eur. Heart J., 2000; 21: 92-94.
11.) Kasaoka S., Tobis J., Akiyama T. et al.: Angiographic and intravascular ultrasound predictors on in-stent restenosis. J. Am. Coll. Cardiol., 1998; 32: 1630-1635.